2013년04월11일 3번
[과목 구분 없음] 다음은 분자량이 104인 탄화수소 X의 분자식을 구하는 원소 분석 실험이다.
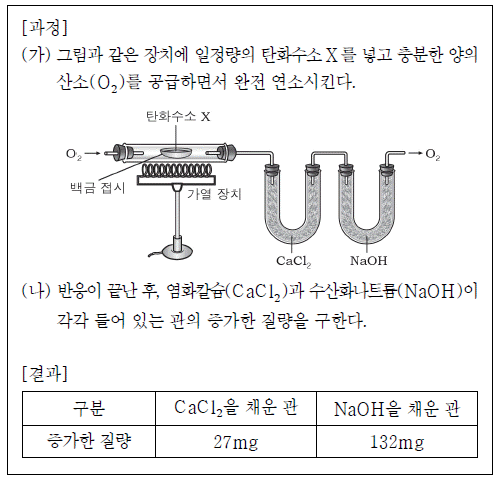
이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, 수소, 탄소, 산소의 원자량은 각각1, 12, 16이다.) [3점]

이에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, 수소, 탄소, 산소의 원자량은 각각1, 12, 16이다.) [3점]

- ① ㄴ
- ② ㄷ
- ③ ㄱ, ㄴ
- ④ ㄱ, ㄷ
- ㄴ, ㄷ
(정답률: 알수없음)
문제 해설
보기에서 정답이 "ㄱ, ㄷ" 인 이유는 다음과 같다.
- 보기 ㄴ: 실험 결과 산소의 질량이 0.5g으로 나왔는데, 이는 산소 분자가 아닌 수소와 결합한 산소의 질량이다. 따라서 이 실험 결과로는 X의 분자식을 구할 수 없다.
- 보기 ㄷ: 실험 결과 탄소의 질량이 2g으로 나왔는데, 이는 탄소 원자 1개가 아닌 탄소 원자 2개가 결합한 형태의 질량이다. 따라서 이 실험 결과로는 X의 분자식을 구할 수 없다.
- 보기 ㄱ: 실험 결과 수소의 질량이 0.5g으로 나왔으므로, 수소 원자 2개가 결합한 형태의 질량이다. 또한 탄소의 질량이 12g으로 나왔으므로, 탄소 원자 1개가 결합한 형태의 질량이다. 이를 이용하여 X의 몰 질량을 계산하면 104g/mol이 된다. 따라서 X의 분자식은 C8H10이 된다.
- 보기 ㄴ: 실험 결과 산소의 질량이 0.5g으로 나왔는데, 이는 산소 분자가 아닌 수소와 결합한 산소의 질량이다. 따라서 이 실험 결과로는 X의 분자식을 구할 수 없다.
- 보기 ㄷ: 실험 결과 탄소의 질량이 2g으로 나왔는데, 이는 탄소 원자 1개가 아닌 탄소 원자 2개가 결합한 형태의 질량이다. 따라서 이 실험 결과로는 X의 분자식을 구할 수 없다.
- 보기 ㄱ: 실험 결과 수소의 질량이 0.5g으로 나왔으므로, 수소 원자 2개가 결합한 형태의 질량이다. 또한 탄소의 질량이 12g으로 나왔으므로, 탄소 원자 1개가 결합한 형태의 질량이다. 이를 이용하여 X의 몰 질량을 계산하면 104g/mol이 된다. 따라서 X의 분자식은 C8H10이 된다.


연도별
- 2016년09월01일
- 2016년07월06일
- 2016년06월02일
- 2016년04월06일
- 2016년03월10일
- 2015년11월12일
- 2015년10월13일
- 2015년09월02일
- 2015년07월09일
- 2015년06월04일
- 2015년04월09일
- 2015년03월11일
- 2014년11월13일
- 2014년10월07일
- 2014년09월03일
- 2014년07월10일
- 2014년06월12일
- 2014년04월10일
- 2014년03월12일
- 2013년11월07일
- 2013년10월08일
- 2013년09월03일
- 2013년07월12일
- 2013년06월05일
- 2013년04월11일
- 2013년03월13일
- 2012년11월08일
- 2012년10월09일
- 2012년09월04일
- 2012년07월11일
- 2012년06월07일
- 2012년04월10일
- 2011년10월12일
- 2011년09월01일
- 2011년07월13일
- 2011년06월02일
- 2011년04월12일
- 2011년02월28일
- 2010년11월18일
- 2010년10월12일
- 2010년09월02일
- 2010년07월08일
- 2010년06월10일
- 2010년04월13일
- 2010년03월12일
- 2009년11월12일
- 2009년10월15일
- 2009년09월03일
- 2009년07월14일
- 2009년06월04일
- 2009년04월15일
- 2009년03월13일
- 2008년11월13일
- 2008년10월16일
- 2008년09월04일
- 2008년07월15일
- 2008년06월04일
- 2008년04월15일
- 2008년03월14일
- 2007년11월15일
- 2007년10월10일
- 2007년09월06일
- 2007년07월12일
- 2007년06월07일
- 2007년03월16일
- 2006년11월16일
- 2006년10월12일
- 2006년09월06일
- 2006년06월03일
- 2006년04월19일
- 2006년03월11일